1超临界干燥研究
超临界流体是一种温度和压力处于临界点以上的无汽液界面区别而兼具液体性质和气体性质的物质相态,它具有特殊的溶解度,易调变的密度,较低的粘度和较高的传质速率,作为溶剂和干燥介质显示出独特的优点和实际应用价值[1]。1931年Kistler[2]首次开创性地采用超临界流体干燥技术(Supereritical fluid drying,SCFD)在不破坏凝胶网络框架结构的情况下,将凝胶中的分散相抽提掉,制得具有很高比表面和孔体积及较低堆密度,折光指数和热导率的块状气凝胶(aerogel monolith)或粉体,并预言了其在催化剂、催化剂载体、绝缘材料、玻璃和陶瓷等诸多方面的潜在应用,但由于制备周期长,设备和一些技术困难,在随后的几十年内一直未引起人们足够的重视。1965年Nieolaon和Teiehner[3]直接采用有机盐制备醇凝胶(aloogel),大大缩短了超临界流体干燥周期;1985年Tewari[4]使用CO2作为超临界流体干燥介质,使超临界温度大为降低,提高了设备的安全可靠性,才使超临界流体干燥技术迅速地向实用化阶段迈进。近年来,SiO2块状气凝胶已成功地用作高能物理实验中的粒子检测器,并生产出具有热绝缘性和太阳能收集作用的夹层窗,尤其引人注目的是气凝胶粉体作为催化剂或其载体已广泛地用于许多催化反应体系[5]。块状气凝胶或粉体作为玻璃和陶瓷的前驱体亦显示出诱人的应用前景。此外,超临界流体干燥技术可有效地克服使凝胶粒子聚集的表面张力效应,所制得的气凝胶粉体常常是由超细粒子(UFP)组成,因而也被认为是制备超细材料的有效方法之一[6]。
不难看出,超临界流体干燥技术为高新技术材料的开发提供了重要的途径和研究方向,发表的论文和专利数量呈现迅速上升趋势。
2 气凝胶及纳米粉体的制备说明
众所周知,凝胶(gel)是胶体粒子或高聚物分子在一定条件下互相连接形成的空间三维网状结构,其孔隙中充满了一种连续相的分散介质。按分散介质的不同,将凝胶分为水凝胶、醇凝胶、离子液体凝胶和气凝胶等。凝胶孔隙中分散介质是水的被称为水凝胶(hyrodegl或aquagel),是醇类的被称为醇凝胶(alcogel),是离子液体的被称为离子液体凝胶(inongel) [7],是气体(通常为空气)的被称为气凝胶(aerogel)。
一般认为,由于湿凝胶在干燥过程中易发生弯曲、变形和开裂,所以要除去这些液态溶剂而保持纤细的多孔网络结构不变是极其困难的,对干燥条件的要求相当苛刻,干燥条件稍有不当,便会导致整个制备过程的失败[8]。因此,制备高质量块状气凝胶的传统方法是超临界干燥技术,其机理是:
当温度和压力达到或超过凝胶孔隙中液体溶剂的超临界值时,孔洞汽-液界面消失,表面张力变得很小甚至消为零。当超临界流体从凝胶孔隙中排出时,不会导致其网络骨架的收缩及结构坍塌,可得到具有凝胶原有结构的块状气凝胶材料。超临界干燥一般采用二氧化碳、甲醇、乙醇等作为干燥介质,表1给出了一些常用超临界干燥介质的临界参数。
表1 一些干燥介质的临界参数及沸点[9-11]
干燥介质 | 临界温度/oC | 临界压力/MPa | 临界密度/g.m-3 | 沸点/oC |
二氧化碳(CO2) | 31.1 | 7.36 | 0.468 | -78.5 |
甲醇(CH3OH) | 239.4 | 7.93 | 0.272 | 64.6 |
乙醇(C2H5OH) | 243 | 6.36 | 0.276 | 78.3 |
水(H2O) | 374.1 | 21.8 | 0.322 | 100 |
正丙醇(1-C3H7OH) | 264 | 5.2 | 0.275 | 97.2 |
异丙醇(i-C3H7OH) | 235.1 | 4.8 | 0.273 | 82.2 |
正丁醇(C4H9OH) | 290 | 4.3 | 0.271 | 117.3 |
丙酮(CH3OC2H5) | 235 | 4.7 | 0.235 | 56.5 |
乙醚(C2H5OC2H5) | 192.5 | 3.6 | 0.265 | 34.6 |
苯(C6H6) | 288.9 | 4.9 | 0.302 | 80.1 |
氮(NH2) | 135.2 | 11.5 | 0.236 | -33.4 |
一氧化二氮(N2O) | 37 | 7.3 | 0.454 | -89 |
纳米ZrO2材料具有优良的力学、热学、电学、光学性质,在功能陶瓷、结构陶瓷、电子陶瓷、传感器、催化剂和高温固体电解质等领域有着广泛的应用。要获得高性能的纳米ZrO2材料,必须制备高质量的纳米ZrO2粉体。在制备纳米ZrO2常用的方法中,化学共沉淀法可以精确控制各组分的含量,使不同组分之间实现分子、原子水平上的混合。而且,反应物溶液浓度高,有较高的粉末产出比,但该方法有可能形成严重的团聚结构,破坏了粉体的性质。一般认为,沉淀、干燥及煅烧处理过程都有可能产生团聚体,如果希望制备出均匀、超细的复合氧化物粉,就必须对制备全过程进行严格的控制。干燥过程也可以采取新工艺,如冷冻干燥、喷雾干燥等,但这些新工艺工艺复杂、设备昂贵、操作周期长且粉料的活性仍不是很高。近年来,人们对超临界流体干燥法制备纳米粒子的研究日益重视,并取得了比较多的研究成果[12]。
在超临界条件下,保持适当时间,由于流体具有极好的渗透性、较低的粘度和高的质量传递速率,在无表面张力的情况下,贫水流体和富水流体相容为C2H5OH-H2O(以C2H5OH为介质)二元均质流体,这样凝胶中的水转移到流体中去,其后在不改变流体状态的等温条件下,缓缓释放流体,最终得到不发生聚集的凝胶粒子,即保持原有结构状态的ZrO2气凝胶超细粉[13]。超临界流体干燥技术可有效地克服使凝胶粒子聚集的表面张力效应,所制得的气凝胶粉体由超细粒子组成,因而也被认为是制备超细材料的有效方法之一。
虽然超临界干燥工艺可以避免孔隙中毛细管压力的破坏[14],获得较为理想的块状气凝胶材料,但其条件苛刻,制备周期耗时长,设备要求高,能耗比较大,这就大大增加了制备块状气凝胶的困难,使块状气凝胶产品的价格极其昂贵,因而极大限制了气凝胶的商品化生产。
3饱水文物的干燥技术
饱水文物的脱水加固是文物保护中的一个重要组成部分,饱水文物被发掘时,内部充满水分,因受地下环境作用和微生物侵蚀,均存在不同程度的降解,有些糟朽十分严重,用手轻轻一按即有水分渗出。为了陈列或考古需要,通常需将这类文物脱水并保存在干燥的环境中。由于文物材质已相当疲弱,为了支撑结构防止干燥时因干燥应力作用而出现收缩和龟裂,通常在干燥前需用填充剂浸渍,通过溶液的自然扩散,让填充剂置换出部分水以改善干燥过程中的内部孔穴塌陷现象。常用填充剂有PEG、甘露醇、酪等物质[15]。
饱水文物的传统脱水方法有:控制特定空间相对湿度的自然干燥法、真空加热干燥法、真空冷冻干燥法。对于含水率不高的文物处理,也有采用溶剂(如醇醚法)置换法,即用挥发性有机溶剂逐渐置换饱水文物中水分以最终达到干燥的目的。为了防止收缩,大多置换溶剂中仍添加填充剂如松香树脂等。以上方法若按干燥工艺可概括为:先浸渍填充剂后干燥法和先浸渍小分子单体后用引发剂或辐照的聚合反应法,这些方法在实际应用中均存在着不同的缺陷,归纳起来有以下方面:(l)文物处理周期长;(2)浸渍处理过程中,因文物结构中的细胞壁内外存在浓度差,将产生渗透压,足以使细胞壁坍塌;(3)引入了外来化合物,永久封存在文物内部,影响对文物的进一步鉴定;(4)存在干燥应力;(5)引发剂含量、反应温度控制不当极易发生爆聚,使文物遭受永久性破坏[16-18]。
超临界CO2干燥技术是近年来发展起来的一种新型分离和脱水干燥技术,它具有安全、快速等特点。在饱水文物的脱水干燥过程中具有以下特点:①当干燥物置于超临界环境中,气/液界面消失,无液相表面张力,干燥过程温和,避免了干燥应力对饱水文物结构的破坏;②由于超临界CO2具有高扩散系数特性,其脱水干燥速度快;③脱水干燥在高压下进行,脱水过程兼有杀菌作用。
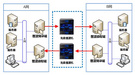
图1是实验室超临界CO2干燥饱水竹木器具的工艺流程图。开始实验前,将需要干燥的固体物料放入萃取干燥釜中,并密封关闭。打开CO2高压储罐,CO2经过滤器进入水冷却箱中(水冷却箱由制冷设备制冷),气态CO2经过冷却后,变成液态CO2,再经高压泵进行压缩,变成超临界CO2流体而进入萃取干燥釜,与含液体溶剂的固体物料接触。固体物料中的液体溶剂溶于超临界CO2中,即固体物料在萃取干燥釜中脱除液体达到干燥。将含有溶剂的CO2通过节流阀进行节流膨胀,压力降到低压,喷入分离釜。此时溶剂在CO2中的溶解度降低,自CO2中析出,汇集于分离釜底部。CO2则从分离釜顶部引出,通过流量计,记录其累积流量和瞬时流量。最后,将萃取干燥釜内CO2缓慢排空至常压后,打开萃取干燥釜,即得干燥后的固体物料,萃取分离的溶剂则从分离釜底部阀门收集